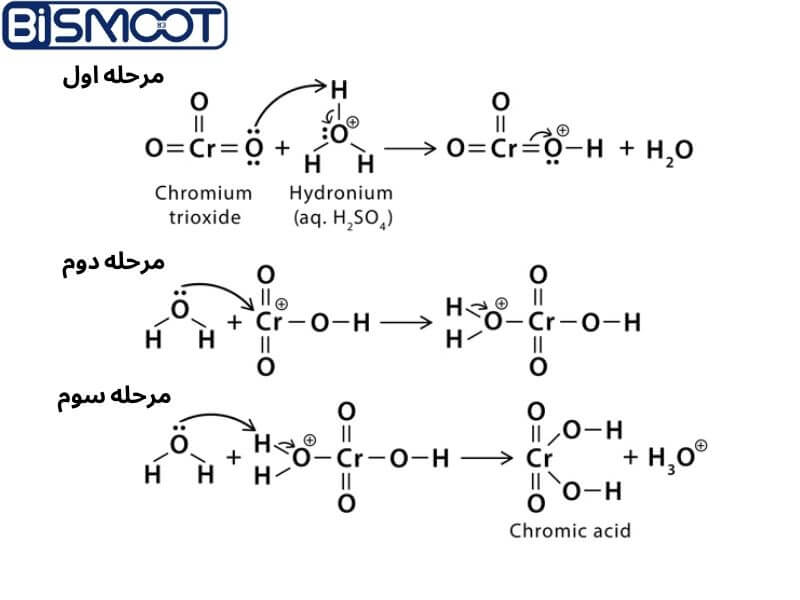
کرومیک اسید، که به عنوان تری اکسید کروم نیز شناخته می شود، یک عامل اکسید کننده قوی است که به طور گسترده در کاربردهای مختلف صنعتی و آزمایشگاهی استفاده می شود. فرمول شیمیایی این ماده CrO3 است و به صورت کریستال ها یا پوسته های قرمز تیره است. اسید کرومیک بسیار خورنده و سمی است، بنابراین، هنگام استفاده از آن باید اقدامات احتیاطی مناسبی را رعایت کرد. در این مقاله، خواص، کاربردها و ملاحظات ایمنی کرومیک اسید را بررسی خواهیم کرد. اگر بعد از مطالعه مقاله اسید کرومیک قصد خرید اسید کرومیک را داشتید، پیشنهاد میکنیم به صفحه ی خرید این ماده مراجعه کنید.
کرومیک اسید چیست؟
کرومیک اسید که با نام تری اکسید کروم (CrO3) نیز شناخته می شود، یک ترکیب معدنی است که حاوی کروم در بالاترین حالت اکسیداسیون (+6) است. این یک اسید قوی و یک عامل اکسید کننده قوی است. اسید کرومیک به صورت کریستال های قرمز روشن ظاهر می شود و به شدت در آب محلول است و آن را به ترکیبی همه کاره در بسیاری از فرآیندهای شیمیایی تبدیل می کند. همچنین این ماده ویژگی های خاصی دارد که باعث کاربرد فراوان این ماده در صنعت شده است. این ویژگی ها عبارتند از:
حالت فیزیکی: اسید کرومیک در حالت جامد به صورت کریستال های قرمز روشن وجود دارد. با این حال، هنگامی که در آب حل می شود، یک محلول قرمز تیره نارنجی تشکیل می دهد.
قدرت اکسید کننده: اسید کرومیک یک عامل اکسید کننده قوی است. این ماده به آسانی اتم های اکسیژن را از دست میدهد و واکنش های اکسیداسیون با سایر مواد را تسهیل می کند.
اسیدیته: اسید کرومیک بسیار اسیدی است و سطح pH آن کمتر از 1 است. میتواند به شدت با برخی ترکیبات آلی واکنش نشان دهد و آن را به یک ماده خطرناک تبدیل کند.
پایداری: اسید کرومیک در شرایط کنترل شده نسبتاً پایدار است. با این حال، وقتی در معرض گرما، نور یا سایر عوامل کاهنده قرار می گیرد، می تواند تجزیه شود.
خواص کرومیک اسید
اسید کرومیک به دلیل رنگ قرمز تیره متمایز و ماهیت اسیدی آن شناخته شده است. در ادامه به برخی از ویژگی های فیزیکی اسید کرومیک می پردازیم:
فرمول شیمیایی: CrO3
جرم مولی: 99.99 گرم بر مول
حالت فیزیکی: کریستال ها یا تکه های قرمز تیره
حلالیت: محلول در آب و برخی از حلالهای آلی
چگالی: 2.7 گرم بر سانتی متر مکعب
نقطه ذوب: 197 درجه سانتی گراد
نقطه جوش: 250 درجه سانتی گراد
تاریخچه اسید کرومیک
اسید کرومیک اولین بار در اوایل قرن نوزدهم توسط شیمیدان فرانسوی لوئیس نیکلاس واکوئلین کشف شد. او تری اکسید کروم را از کروکویت، یک کانی سرب قرمز جدا کرد. این کشف پیشگامانه راه را برای مطالعه گسترده اسید کرومیک و کاربردهای آن در زمینه های مختلف هموار کرد.
کاربرد اسید کرومیک چیست؟
اسید کرومیک به دلیل خاصیت اکسید کنندگی قوی در صنایع و آزمایشگاه های مختلف کاربرد فراوانی پیدا می کند. برخی از کاربردهای رایج آن عبارتند از:
آبکاری و تکمیل فلز
اسید کرومیک به طور گسترده در صنعت آبکاری و تکمیل فلزات استفاده می شود. از این ماده به عنوان یک جزء کلیدی در تهیه پوشش های کروم اندود روی سطوح مختلف فلزی استفاده می شود. این پوشش ها سبب مقاومت در برابر خوردگی می شود، ظاهر اجسام را بهبود می بخشند و دوام آنها را افزایش می دهند. محصولاتی مانند قطعات خودرو، لوازم حمام و اقلام تزئینی اغلب تحت پوشش اسید کرومیک قرار می گیرند. این فرآیند شامل فرو بردن جسم فلزی در محلولی حاوی اسید کرومیک و اعمال جریان الکتریکی است. این منجر به رسوب یک لایه نازک و مقاوم در برابر خوردگی از کروم بر روی سطح فلز می شود.
صنعت عکاسی
در حوزه عکاسی، کرومیک اسید از لحاظ تاریخی برای تولید فیلم های سیاه و سفید استفاده می شده است. این کمک می کند تا تصویر نهفته گرفته شده روی فیلم را به یک تصویر قابل مشاهده تبدیل کند. در حالی که استفاده از آن با ظهور عکاسی دیجیتال کاهش یافته است، اهمیت آن در تاریخ صنعت عکاسی غیرقابل انکار است.
عامل تمیز کننده
اسید کرومیک یک عامل تمیز کننده و حکاکی موثر برای طیف وسیعی از مواد است. معمولاً برای از بین بردن بقایای آلی، زنگ زدگی و رسوب از سطوح فلزی استفاده می شود. علاوه بر این، می تواند شیشه و سرامیک را حکاکی کند و در ساخت بردهای مدار چاپی و دستگاه های نیمه هادی مفید باشد.
کاتالیزور
کرومیک اسید نیز به عنوان یک کاتالیزور در واکنش های شیمیایی مختلف استفاده می شود. وجود آن می تواند به طور قابل توجهی سرعت واکنش و بازده فرآیندهای خاص را افزایش دهد. به عنوان مثال، در سنتز ترکیبات آلی، واکنش های اکسیداسیون و تولید رنگ ها و رنگدانه ها استفاده می شود. خواص کاتالیزوری اسید کرومیک آن را به ابزاری ارزشمند در صنایع شیمیایی تبدیل کرده است.
شیمی تجزیه
در زمینه شیمی تجزیه از کرومیک اسید به عنوان یک معرف برای آزمایش ها و آنالیزهای مختلف استفاده می شود. به ویژه در آزمایش وجود آلدئیدها و الکل ها مفید است. اسید کرومیک با این ترکیبات آلی واکنش می دهد و تغییرات رنگ مشخصی ایجاد می کند یا رسوب می دهد که به شناسایی مواد مورد آزمایش کمک می کند. همچنین اسید کرومیک می تواند الکل های اولیه را به آلدئید و الکل های ثانویه را به کتون تبدیل کند. علاوه بر این، کرومیک اسید در اکسیداسیون برخی از گروه های عاملی مانند سولفیدها به سولفوکسیدها و تیول ها به دی سولفیدها استفاده می شود.
آزمایش کرومات
اسید کرومیک نقش حیاتی در آزمایش و آنالیز کرومات ها، که ترکیبات حاوی یون کرومات (CrO4^2-) هستند، ایفا می کند. این آزمایش ها شامل افزودن اسید کرومیک به نمونه است که منجر به تغییر رنگ یا تشکیل رسوب می شود. این واکنش ها برای شناسایی و تعیین کمیت حضور کرومات ها در نمونه های مختلف از جمله آب، خاک و پساب های صنعتی استفاده می شود.
نگهدارنده چوب
اسید کرومیک به عنوان نگهدارنده چوب برای محافظت در برابر پوسیدگی و هجوم حشرات استفاده می شود. می توان آن را برای سازه های چوبی مانند تیرهای برق اعمال کرد و طول عمر آنها را افزایش داد و یکپارچگی ساختاری آنها را تضمین کرد. با این حال، به دلیل ماهیت سمی آن، استفاده از اسید کرومیک به عنوان نگهدارنده چوب در بسیاری از کشورها به شدت تحت نظارت است.
کروماتوگرافی
اسید کرومیک به عنوان یک فاز ثابت در تکنیک های کروماتوگرافی خاص، به ویژه در کروماتوگرافی تبادل یونی استفاده می شود. این به جداسازی و تجزیه و تحلیل یونها بر اساس میل آنها به فاز ساکن کمک میکند و امکان شناسایی و تعیین کمیت مواد مختلف را فراهم میکند. این نرم افزار به طور گسترده در آزمایشگاه های تحقیقاتی و بخش های کنترل کیفیت استفاده می شود.
روش های تولید اسید کرومیک
روش های مختلفی برای تولید اسید کرومیک وجود دارد. بیایید برخی از روش های رایج مورد استفاده را بررسی کنیم:
- روش اسید سولفوریک
در روش اسید سولفوریک، دی کرومات سدیم با اسید سولفوریک غلیظ تصفیه می شود. این واکنش باعث تولید اسید کرومیک و سولفات سدیم به عنوان یک محصول جانبی می شود. سپس اسید کرومیک جدا شده و طی مراحل بعدی خالص سازی می شود.
- روش کرومیل کلرید
روش کرومیل کلرید شامل واکنش سنگ معدن کرومیت با کلرید سدیم و اسید سولفوریک غلیظ است. این واکنش باعث تولید کرومیل کلرید می شود که متعاقباً هیدرولیز می شود تا اسید کرومیک بدست آید.
- روش دی کرومات سدیم
در روش دی کرومات سدیم، کرومات سدیم ابتدا از بو دادن سنگ معدن کرومیت با کربنات سدیم و آهک تولید می شود. سپس کرومات سدیم با اسید سولفوریک اسیدی می شود تا دی کرومات سدیم تولید شود. در نهایت، دی کرومات سدیم با اسید سولفوریک واکنش داده تا اسید کرومیک بدست آید.
- روش کرومیک انیدرید
روش انیدرید کرومیک شامل آبگیری اسید کرومیک با استفاده از اسید سولفوریک یا اسید فسفریک است. این فرآیند باعث ایجاد انیدرید کروم می شود که می تواند در آب حل شود و اسید کرومیک بدست آید.
- روش الکترولیز
در روش الکترولیز، از یک سلول الکترولیتی برای تولید اسید کرومیک از محلول کرومات سدیم یا دی کرومات سدیم استفاده می شود. این روش مزیت تولید مستقیم را بدون نیاز به واکنش های شیمیایی اضافی ارائه می دهد.
سوالات متداول
آیا می توان از اسید کرومیک برای تمیز کردن ظروف شیشه ای استفاده کرد؟
از اسید کرومیک می توان برای تمیز کردن ظروف شیشه ای استفاده کرد، اما این ماده بسیار خورنده است و باید با احتیاط رفتار کرد. برای تمیز کردن معمولی ظروف شیشه ای توصیه می شود از مواد پاک کننده جایگزین استفاده کنید که خطر کمتری دارند.
آیا اسید کرومیک می تواند باعث سوختگی پوست شود؟
بله، کرومیک اسید در صورت تماس می تواند باعث سوختگی شدید پوست شود. پوشیدن دستکش و لباس محافظ هنگام استفاده از اسید کرومیک برای جلوگیری از قرار گرفتن در معرض پوست ضروری است.
جایگزین های اسید کرومیک در آبکاری فلز چیست؟
با توجه به نگرانی های زیست محیطی و بهداشتی مرتبط با اسید کرومیک، روش های آبکاری جایگزین با استفاده از ترکیبات دیگر، مانند محلول های کروم سه ظرفیتی، برای جایگزینی اسید کرومیک در فرآیندهای آبکاری فلزات ایجاد شده است.
جمع بندی
کرومیک اسید که به عنوان تری اکسید کروم نیز شناخته می شود، یک عامل اکسید کننده قوی با کاربردهای مختلف صنعتی و آزمایشگاهی است. از این ماده در شیمی تجزیه، نگهداری چوب، ابکاری و … کاربرد های فراوانی دارد. با این حال، به دلیل خواص خورنده و سمی آن، مراقبت از اسید کرومیک بسیار مهم است. ما در این مقاله از شرکت بیسموت برای شما اطلاعات مفیدی از چیستی، کاربرد و روش های تولید این ماده جمع آوری کرده ایم و امیدواریم این مقاله برای شما مفید بوده باشد.