حلال های شیمیایی
انواع حلال های شیمیایی به ماده ای اطلاق می شود که قادر به حل کردن ماده دیگری باشد. به طور کلی هیچ واکنشی بین حلال و املاح رخ نمی دهد و ماده جدیدی تولید نمی شود. به عنوان مثال، هنگامی که آب در یک ماده قطبی حل می شود، مولکول های آب به دلیل نیروی وارد شده توسط حلال وارد مولکول های آب می شوند. آنها جدا شده و بین مولکول های حلال قرار می گیرند.
حلال های شیمیایی معمولاً در دمای محیط مایع هستند، اما در جامد (حلال های یونی) یا گاز (دی اکسید کربن) نیز وجود دارند. حل کردن یک ماده در یک ترکیب دیگر برای اهداف مختلفی از جمله تنظیم ویسکوزیته، تغییر خواص دما، حذف یک ماده از یک سطح خاص، استخراج یک ماده و غیره قابل انجام است.
حلال های آلی
این ترکیبات از نظر ساختار شیمیایی به سه دسته هیدروکربن، اکسیژن و هالوژن تقسیم می شوند.
حلال های هیدروکربنی
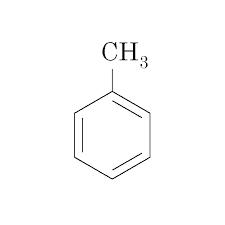
این مواد به دو دسته آلیفاتیک و آروماتیک (بنزن، تولوئن، زایلن و …) تقسیم می شوند. این حلال ها عموماً از نفت خام استخراج می شوند و در برخی موارد از ترکیب مواد مختلف استفاده می شود. به عنوان مثال، پارافین های خطی ویسکوزیته پایینی دارند، در حالی که پارافین های شاخه دار ویسکوزیته بالایی دارند و خواص دمای پایین خوبی دارند. ترکیب این حلال ها ویسکوزیته خوب و خواص دمای پایین خوبی به ما می دهد.
حلال های اکسیژن
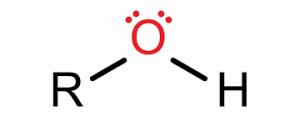
این حلال ها عبارتند از الکل ها، کتون ها، آلدئیدها، گلیکول اترها، استرها و غیره.
حلال های هالوژن
موادی که در ساختار گروه هالوژن خود عنصری دارند (کلر، برم و …) هالوژن نامیده می شوند.